华中科技大学杨祥良/甘璐开发新的微粒,引发化疗诱导的抗肿瘤免疫级联扩增,以促进抗PD-1治疗!

免疫检查点阻断(ICB)疗法,特别是针对程序性死亡受体1 (PD-1)及其配体(PD-L1)的抗体,已经彻底改变了癌症治疗。然而,它作为一种独立疗法的疗效仍然有限。尽管ICB联合化疗显示出良好的治疗效果,但挑战在于如何有效地放大化疗诱导的抗肿瘤免疫。这依赖于有效的药物递送到肿瘤细胞和树突状细胞(DCs)强大的抗原呈递。
2023年10月25日,华中科技大学杨祥良及甘璐共同通讯在Signal Transduction and Targeted Therapy(IF=39)在线发表题为“Tumor-repopulating cell-derived microparticles elicit cascade amplification of chemotherapy-induced antitumor immunity to boost anti-PD-1 therapy”的研究论文,该研究开发了肿瘤再生细胞(TRC)衍生的微粒,具有特殊的肿瘤靶向性,可递送阿霉素(DOX@3D-MPs),以改善抗PD-1治疗。
DOX@3D-MPs有效诱导免疫原性肿瘤细胞死亡,释放足够的肿瘤抗原。热休克蛋白70 (HSP70)在DOX@3D-MPs中过表达有助于捕获肿瘤抗原,促进其被DCs吞噬,促进DCs成熟,导致CD8+ T细胞活化。DOX@3D-MPs显著提高抗PD-1治疗对大皮下H22肝癌、原位4T1乳腺肿瘤和Panc02胰腺肿瘤模型的疗效。这些结果表明,DOX@3D-MPs有望作为药物提高ICB治疗的应答率,并产生持久的免疫记忆,以防止肿瘤复发。

免疫检查点阻断(ICB)疗法,以抗程序性死亡受体1/程序性死亡受体配体(PD-1/PD-L1)抗体为例,旨在重新激活T细胞介导的抗肿瘤免疫来对抗肿瘤细胞,是一种有效的治疗方法。虽然抗PD-1/抗PD-L1治疗提供了类似于治愈的潜在临床效果,但只有部分患者(20-30%)有望从抗PD-1/抗PD-L1治疗中获益。此外,先天或获得性耐药的发展最终可能导致最初反应良好的患者的癌症进展,解决治疗耐药的局限性是推进ICB治疗临床应用的重大挑战。ICB治疗的低应答率主要归因于遇到“免疫冷”肿瘤,其特征是免疫原性有限,肿瘤浸润淋巴细胞不足或终末耗尽,肿瘤免疫微环境(TIM)受到抑制。
许多努力将“免疫冷”肿瘤转化为“免疫热”肿瘤的方法已被提出,以增强ICB治疗的有效性,包括与化疗、放疗、抗血管生成治疗、靶向治疗等现有治疗方法的联合治疗化疗是癌症治疗的经典策略之一,通过诱导肿瘤细胞发生免疫原性细胞死亡(immunogenic cell death, ICD) ,促进免疫调节分子和肿瘤抗原的释放,激活树突状细胞(dendritic cells, DCs)增加抗原交叉递呈,可以直接杀伤肿瘤细胞,同时正向调节抗肿瘤免疫。同时,化疗还可以触发CXCL10等趋化因子的分泌,将T细胞和记忆T细胞募集到TIM。此外,化疗可以通过减少免疫抑制细胞的存在,如调节性T细胞(Tregs)和髓源性抑制细胞(MDSCs),改善肿瘤免疫抑制微环境。
然而,传统的化疗药物可能无法达到预期的ICD效果,因为药物传递到肿瘤细胞的能力差此外,DCs的抗原呈递不足导致T细胞激活不足。因此,开发有效的化疗递送系统,增强DCs的肿瘤细胞靶向和抗原呈递,对于推进ICB治疗和化疗的联合治疗效益具有很大的希望。
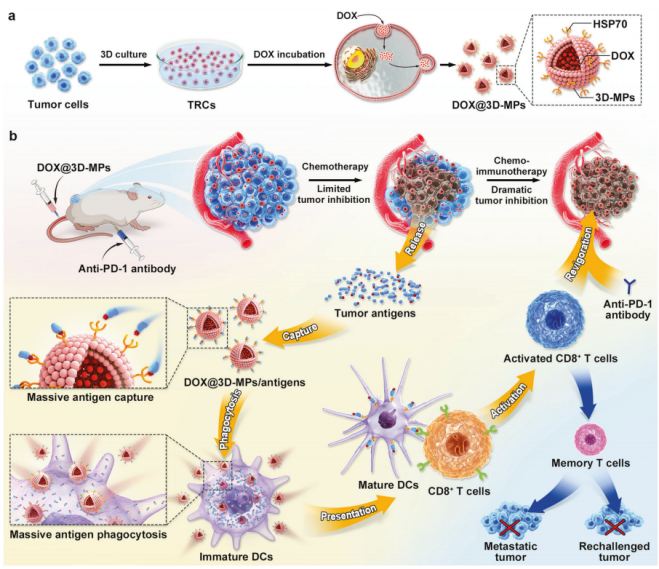
DOX@3D-MPs作为抗PD-1抗体治疗的有效增强剂示意图。图自:Signal Transduction and Targeted Therapy
细胞源性细胞外囊泡(EVs),如微颗粒(MPs)和外泌体,由于先天的细胞或组织特异性归巢能力、良好的生物安全性和可忽略的免疫原性,作为药物运输系统表现出潜在的优势。同时,细胞源性EVs继承了供体细胞的信号分子,表现出独特的生物学特性。之前的工作表明,肿瘤细胞源性外泌体通过过表达细胞间粘附分子-1 (ICAM-1, CD54)有效靶向肿瘤。
最近,作者开发了一种基于肿瘤再生细胞(TRC)衍生的MPs (3D-MPs)的药物输送系统,用于输送抗癌药物,以增强癌症治疗。由于细胞骨架相关蛋白cytospin-A的低表达,3D-MPs具有独特的柔软性和可变形性,可以增加药物在肿瘤中的积累,成功地从肿瘤血管扩散,有效地渗透到肿瘤组织深处,并有效地将抗癌药物内化到肿瘤细胞和TRCs中。除了改进的肿瘤靶向药物输送能力之外,基于3D-MPs的药物输送系统对抗肿瘤免疫的贡献程度还需要进一步的研究。该研究揭示了3D-MPs递送抗癌药物阿霉素(DOX@3D-MPs)有效地激发肿瘤细胞的ICD效应,释放大量免疫调节因子和肿瘤抗原。
更重要的是,DOX@3D-MPs中上调的热休克蛋白70 (HSP70)在捕获肿瘤抗原并促进DCs吞噬肿瘤抗原中发挥重要作用,进而增强DCs的抗原呈递能力,激活肿瘤特异性CD8+ T细胞。因此,DOX@3D-MPs显著提高抗PD1抗体的抗癌功效,诱导持久的免疫记忆,有效地减少肿瘤复发。
来源:iNature
-
生物医药领域要点速览

生物医药领域要点速览
-
Cell Res:把肝癌变成“慢病”!厦门大学林圣彩等团队发现“辟谷精”为肝癌治

Cell Res:把肝癌变成“慢病”!厦门大学林圣彩等团队发现“辟谷精”为肝癌治
-
Nature全新子刊—Nature Hearth,上线首篇论文!

Nature全新子刊—Nature Hearth,上线首篇论文!
-
《科学》:癌细胞喜欢“酸”的原因找到了!这种环境让肿瘤生长更猛烈!

《科学》:癌细胞喜欢“酸”的原因找到了!这种环境让肿瘤生长更猛烈!
-
CRM:这思路,绝了!中国医大/浙大/复旦团队,将中性粒细胞变成“顺风车”,搭载

CRM:这思路,绝了!中国医大/浙大/复旦团队,将中性粒细胞变成“顺风车”,搭载