铁死亡 | Adv Sci :中南大学陶永光/肖德胜/刘双发现铁死亡和细胞焦亡相互作用新机制!
各种形式的程序性细胞死亡(PCD)根据其特定的分子机制表现出不同的特征,且不同形式间存在相互作用。铁死亡与自噬和细胞凋亡相关,但尚不清楚其与焦亡之间的潜在相互作用。
2024年1月4日,中南大学陶永光、肖德胜及刘双共同通讯(王海燕为第一作者)在Advanced Science在线发表题为“BRCC36 Deubiquitinates HMGCR to Regulate the Interplay Between Ferroptosis and Pyroptosis”的研究论文,该研究揭示了铁死亡和焦亡之间的相互拮抗关系,其中3-羟基-3-甲基戊二酰辅酶A还原酶(HMGCR)在两者的相互作用中起关键作用。研究发现,HMGCR在铁死亡过程中主要定位于线粒体,但在被焦亡诱导剂处理后转移到内质网。研究表明,BRCC36(含BRCA1/BRCA2的复合亚基36)依赖于去泛素化酶(DUB)活性的方式对HMGCR进行去泛素化,抑制铁死亡并促进细胞焦亡。
BRCC36作为肝细胞癌(HCC)的致癌基因,促进癌细胞增殖、迁移、侵袭和肿瘤生长。Thiolutin是BRCC36的抑制剂,可有效抑制BRCC36与HMGCR之间的相互作用,从而抑制HCC生长。因此,靶向BRCC36是HCC治疗的一种有效策略。综上所述,该发现为进一步表征肿瘤异质性提供了新的理论证据,并为HCC的诊断和治疗提供了新的分子靶点。

细胞死亡对调节多种生理过程和维持机体稳态具有重要意义。近期研究表明,不同形式的程序性细胞死亡(PCD)之间存在串扰。铁死亡是由细胞膜中氧化磷脂大量积累引发的铁依赖性细胞死亡,在细胞形态、生化特征和遗传调控方面与其他类型的PCD不同。各种研究表明,铁死亡与经元变性、各种类型的癌症(如肝癌、肺癌、结肠癌和胰腺癌)等生理和病理过程有关。多种癌症类型中,激活全身性Xc转运蛋白、谷胱甘肽(GSH)代谢增加、谷胱甘肽过氧化物酶(GPX4)活性增强以及抑制脂质过氧化和铁代谢能够抑制铁死亡。
脂质过氧化物的积累是铁死亡的关键标志,而GPX4是促进GSH转化为氧化谷胱甘肽(GSSG)的基本调节分子,继而消除损伤细胞的脂质过氧化物。HMGCR是甲羟戊酸产生的限速酶,通过增强GPX4和辅酶Q10(CoQ10)的合成来抑制铁死亡。GSH-GPX4、GCH1(GTP依赖性环水解酶1)-BH4(四氢生物蝶呤)、NADPH-FSP1(铁死亡抑制蛋白1)-辅酶Q10和 DHODH(二氢乳清酸脱氢酶)-辅酶Q10通路是调节细胞对铁死亡敏感性的主要抗氧化系统。当GPX4、FSP1、GCH1和其他抗氧化系统受到抑制时,细胞发生铁死亡。最新研究表明,铁死亡与各种形式的程序性细胞死亡之间存在串扰。如铁蛋白自噬、脂肪自噬、自噬、线粒体自噬和伴侣介导的自噬等特异性自噬方式,均能够通过增加游离铁或脂质积累水平来促进铁死亡。
该团队已有研究报道,核长链非编码RNA LINC00618依赖于细胞凋亡促进铁死亡。此外,铁死亡诱导剂青蒿琥酯诱导内质网(ER)应激反应,在介导铁死亡和细胞凋亡之间的串扰中起重要作用。坏死性凋亡和铁死亡之间存在显着的相互作用,其中坏死性凋亡的激活有助于诱导缺血性卒中铁死亡。
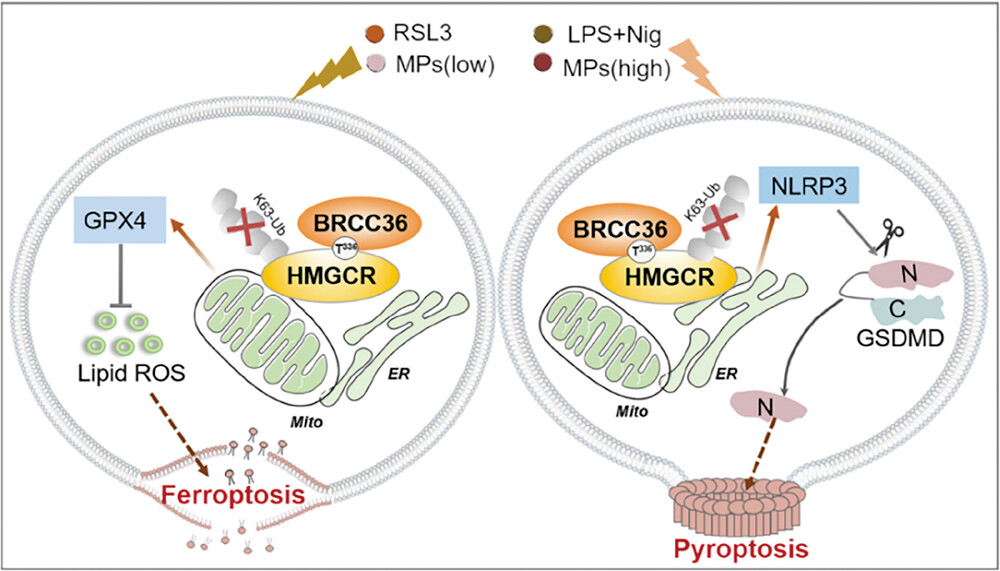
BRCC36去泛素化HMGCR以调节铁死亡和焦亡之间的相互作用(摘自Advanced Science )
细胞焦亡是由 gasdermin 家族蛋白驱动的一种程序性细胞死亡裂解形式,可导致细胞质肿胀和炎症介质(如IL-1β和IL-18)的释放。除DFNB59外,gasdermins(GSDMA-GSDME)是细胞焦亡的主要作用因子。gasdermins的蛋白水解裂解释放N端片段,在膜中形成大的寡聚孔,进一步破坏细胞膜的完整性,最终导致细胞死亡。当细胞受到外部刺激(包括细菌、病毒、毒素)并在胞质溶胶中产生活性N末端片段(GSDMD-N)时,GSDMD可被炎性半胱天冬酶裂解。GSDMD-N识别并插入细胞膜,有助于孔形成和焦亡细胞死亡。
研究表明,颗粒酶还可以通过直接裂解gasdermins来诱导细胞焦亡。细胞焦亡不仅与病毒性疾病有关,对癌症和中枢神经系统疾病也有重大影响。细胞焦亡在癌症中的作用是多方面的:一方面,细胞焦亡有可能阻碍肿瘤的发展;另一方面,细胞焦亡可以刺激建立有利于癌症发展的微环境,促进肿瘤生长。先前的研究表明,脂质过氧化的主要产物4-HNE(4-羟基壬烯醛)可抑制巨噬细胞中NLRP3(NOD样受体热蛋白结构域相关蛋白3)炎症小体活化和焦亡。铁诱导的活性氧(ROS)可以氧化线粒体外膜蛋白Tom20,从而促进Bax向线粒体的募集并刺激caspase-3/GSDME介导的细胞焦亡。总之,铁死亡和焦亡之间存在潜在联系,但尚不清楚其相互作用机制。由BRCC3基因编码的去泛素化酶BRCC36是JAMM家族的成员,其能够特异性地去除与靶蛋白相连的K63多泛素链(K63-UB),但BRCC36是否具有DNA损伤修复和免疫反应之外的其他功能仍有待探索。该研究探讨了铁死亡和焦亡之间的关系,发现二者之间存在拮抗作用。
值得注意的是,作者发现HMGCR在铁死亡和焦亡之间的相互作用中起着至关重要的作用。BRCC36 依赖于DUB活性对HMGCR进行去泛素化,并在促进细胞焦亡的同时抑制铁死亡。此外,BRCC36抑制剂thiolutin可以延缓HCC的进展,表明BRCC36可以作为HCC的治疗靶点。综上所述,该研究为进一步表征肿瘤异质性提供了新的理论证据,并为HCC的诊断和治疗提供了新的分子靶点。
-
生物医药领域要点速览

生物医药领域要点速览
-
Cell Res:把肝癌变成“慢病”!厦门大学林圣彩等团队发现“辟谷精”为肝癌治

Cell Res:把肝癌变成“慢病”!厦门大学林圣彩等团队发现“辟谷精”为肝癌治
-
Nature全新子刊—Nature Hearth,上线首篇论文!

Nature全新子刊—Nature Hearth,上线首篇论文!
-
《科学》:癌细胞喜欢“酸”的原因找到了!这种环境让肿瘤生长更猛烈!

《科学》:癌细胞喜欢“酸”的原因找到了!这种环境让肿瘤生长更猛烈!
-
CRM:这思路,绝了!中国医大/浙大/复旦团队,将中性粒细胞变成“顺风车”,搭载

CRM:这思路,绝了!中国医大/浙大/复旦团队,将中性粒细胞变成“顺风车”,搭载