铁死亡-上海交大苏冰团队揭示CD8+T细胞抵抗铁死亡新机制,带来抗肿瘤免疫新思路!
维持足够的外周CD8+T细胞数量对于建立强大的宿主免疫应答以对抗病原体感染至关重要,抗肿瘤免疫应答的有效性也与浸润在肿瘤微环境中的功能性CD8+T细胞数量呈正相关。外周CD8+T细胞数量受到体内平衡机制的严格调控,以保持整个成年期的总体规模相对恒定,但调控这一过程的确切分子机制仍不完全清楚。
2024年5月20日,上海交通大学医学院上海市免疫学研究所苏冰团队在 Cell Discovery 期刊发表了题为:DEPDC5 protects CD8+ T cells from ferroptosis by limiting mTORC1-mediated purine catabolism 的研究论文。
该研究将DEPDC5介导的mTORC1信号通路与CD8+T细胞对铁死亡的抵抗联系起来,揭示了DEPDC5在保护CD8+T细胞细胞免受活性氧(ROS)诱导的铁死亡中的新作用,从而提出了一种通过抑制CD8+T细胞铁死亡来增强抗肿瘤免疫的新策略。

维持足够的外周CD8+T细胞数量对于建立强大的宿主免疫应答以对抗病原体感染至关重要,抗肿瘤免疫应答的有效性也与浸润在肿瘤微环境中的功能性CD8+T细胞数量呈正相关。外周CD8+T细胞数量受到体内平衡机制的严格调控,以保持整个成年期的总体规模相对恒定,但调控这一过程的确切分子机制仍不完全清楚。
2024年5月20日,上海交通大学医学院上海市免疫学研究所苏冰团队在 Cell Discovery 期刊发表了题为:DEPDC5 protects CD8+ T cells from ferroptosis by limiting mTORC1-mediated purine catabolism 的研究论文。
该研究将DEPDC5介导的mTORC1信号通路与CD8+T细胞对铁死亡的抵抗联系起来,揭示了DEPDC5在保护CD8+T细胞细胞免受活性氧(ROS)诱导的铁死亡中的新作用,从而提出了一种通过抑制CD8+T细胞铁死亡来增强抗肿瘤免疫的新策略。
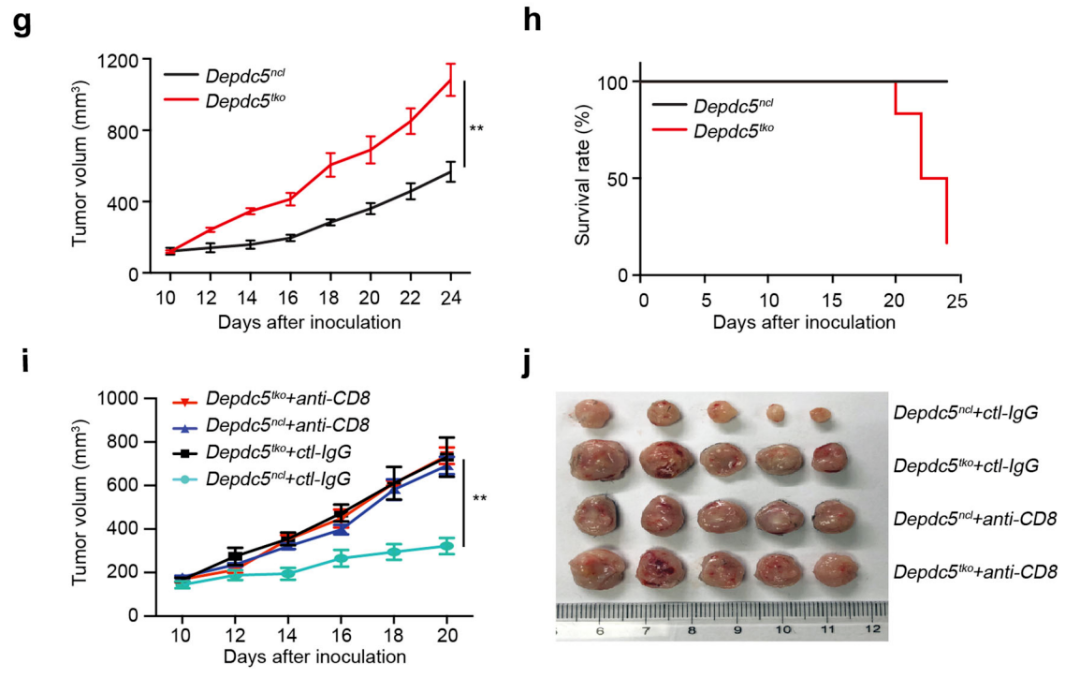
DEPDC5维持外周CD8+T细胞数量和抗肿瘤免疫能力
在机制上,DEPDC5缺陷导致了CD8+T细胞的mTORC1活性增强,从而诱导ATF4表达,进而增加黄嘌呤氧化酶(XO)和脂质ROS的表达,导致自发性铁死亡。
综上所述,该研究将DEPDC5介导的mTORC1信号通路与CD8+T细胞对铁死亡的抵抗联系起来,揭示了DEPDC5在保护CD8+T细胞免受ROS诱导的铁死亡中的新作用,从而提出了一种通过抑制CD8+T细胞铁死亡来增强抗肿瘤免疫的新策略。
来源:生物世界
-
生物医药领域要点速览

生物医药领域要点速览
-
Cell Res:把肝癌变成“慢病”!厦门大学林圣彩等团队发现“辟谷精”为肝癌治

Cell Res:把肝癌变成“慢病”!厦门大学林圣彩等团队发现“辟谷精”为肝癌治
-
Nature全新子刊—Nature Hearth,上线首篇论文!

Nature全新子刊—Nature Hearth,上线首篇论文!
-
《科学》:癌细胞喜欢“酸”的原因找到了!这种环境让肿瘤生长更猛烈!

《科学》:癌细胞喜欢“酸”的原因找到了!这种环境让肿瘤生长更猛烈!
-
CRM:这思路,绝了!中国医大/浙大/复旦团队,将中性粒细胞变成“顺风车”,搭载

CRM:这思路,绝了!中国医大/浙大/复旦团队,将中性粒细胞变成“顺风车”,搭载