张清媛教授:CAPItello-291研究荣登NEJM后再更新,首创AKT抑制剂公布安全性结果
2023年6月2日至6日,美国临床肿瘤学会(ASCO)大会在美国芝加哥盛大召开。CAPItello-291研究携安全性分析结果再次登场 (摘要号:1067) 1。此次大会披露的数据表明Capivasertib+氟维司群的安全性良好,不良事件(AE)可管可控。作为AKT抑制剂+内分泌治疗领域的首个Ⅲ期研究,CAPItello-291研究旨在满足HR+/HER2-晚期乳腺癌内分泌耐药患者的治疗需求,其研究结果先后在2022年圣安东尼奥乳腺癌会议(SABCS)2、2023年欧洲肿瘤内科学会乳腺癌大会(ESMO BC)3等国际大会上重磅公布,并于今年6月1日全文发表在《新英格兰医学杂志》4。CAPItello-291研究的突破性结果备受业界瞩目,Capivasertib显示出了成为First-in-Class AKT抑制剂的巨大潜力。
此次研究亮相ASCO再次引发学者热烈关注,值此之际,医脉通特邀哈尔滨医科大学附属肿瘤医院张清媛教授深入解读CAPItello-291研究最新数据,探讨AKT抑制剂在HR+/HER2-晚期乳腺癌中的应用前景。
大约70%的晚期乳腺癌为HR+/ HER2-乳腺癌5,目前主要的治疗手段是内分泌治疗和CDK4/6抑制剂等,然而大多数患者的疾病仍会进展并产生耐药性,≥2线治疗选择有限,是临床治疗的一大挑战。关于耐药机制,有研究发现PI3K/AKT/mTOR信号通路在乳腺癌中存在广泛激活,与乳腺癌发生、发展以及耐药密切相关6-7。
Capivasertib是针对AKT全部亚型(AKT1/2/3)的强效选择性抑制剂。临床前研究已证实Capivasertib联合氟维司群在AKT通路改变与未改变、未接受CDK4/6抑制剂治疗与CDK4/6抑制剂耐药的模型中均有效8。同时,AKT和ER通路之间存在交互作用,这表明同时抑制两种通路可能会改善治疗疗效,联合治疗的获益与突变状态无关。故无论AKT通路状态如何,乳腺癌患者均可能从Capivasertib联合氟维司群治疗中获益。
此外,PI3K/AKT/mTOR信号通路抑制剂的安全性也是临床关注的问题,一方面是因为PI3K-AKT信号通路对糖代谢有重要的调控作用,相关抑制剂可能影响患者血糖水平;另一方面,既往多项AKT抑制剂的临床研究因安全事件风险而先后折戟9;另外,其他PI3K/mTOR通路抑制剂也有一些安全性风险报道。基于以上背景,肯定Capivasertib疗效的同时,其安全性也是我们需要关注的。
CAPItello-291研究是一项全球、多中心、双盲、随机对照的Ⅲ期研究,旨在评估Capivasertib联合氟维司群用于芳香化酶抑制剂(AI)耐药的HR+/HER2-晚期乳腺癌的疗效与安全性。
截至2022年8月15日,该研究共纳入708例绝经前/绝经后女性及男性HR+/HER2-晚期乳腺癌患者,所有患者均在AI治疗期间或治疗后出现疾病复发或进展,且在晚期阶段既往化疗线数≤1,既往内分泌治疗线数≤2。患者既往未接受过选择性雌激素受体降解剂(SERD)或PI3K/AKT/mTOR抑制剂治疗。
患者随机(1:1)分配接受Capivasertib(400mg PO,连续4d,间隔3d)+氟维司群(500mg IV,前三次注射每14天一次,之后每28天一次)或安慰剂+氟维司群治疗。一个周期定义为连续4周使用Capivasertib或安慰剂。研究以总体人群和伴有AKT通路异常(携带PIK3CA/AKT1/PTEN基因突变)患者的PFS为主要双终点,次要终点包括总体人群和伴有AKT通路异常患者的总生存期(OS)、客观缓解率(ORR)及安全性等。
CAPItello-291研究达到双重主要终点,伴或不伴有AKT通路异常患者均有显著获益
在入组的708名患者晚期乳腺癌中,289名患者(40.8%)伴有AKT通路异常,489名(69.1%)既往接受过CDK4/6抑制剂治疗。结果显示:
在总人群中,Capivasertib+氟维司群组与对照组患者中位PFS分别为7.2个月和3.6个月(HR=0.60;95%CI 0.51–0.71;p<0.001);
在伴有AKT通路异常的患者中,Capivasertib+氟维司群组与对照组中位PFS分别为7.3个月和3.1个月(HR=0.50;95%CI 0.38–0.65;p<0.001);
在不伴有AKT通路异常的患者中,Capivasertib+氟维司群组患者的PFS获益依旧显著(7.2个月vs 3.7个月,HR=0.70;95%CI 0.56–0.88;p<0.001)。
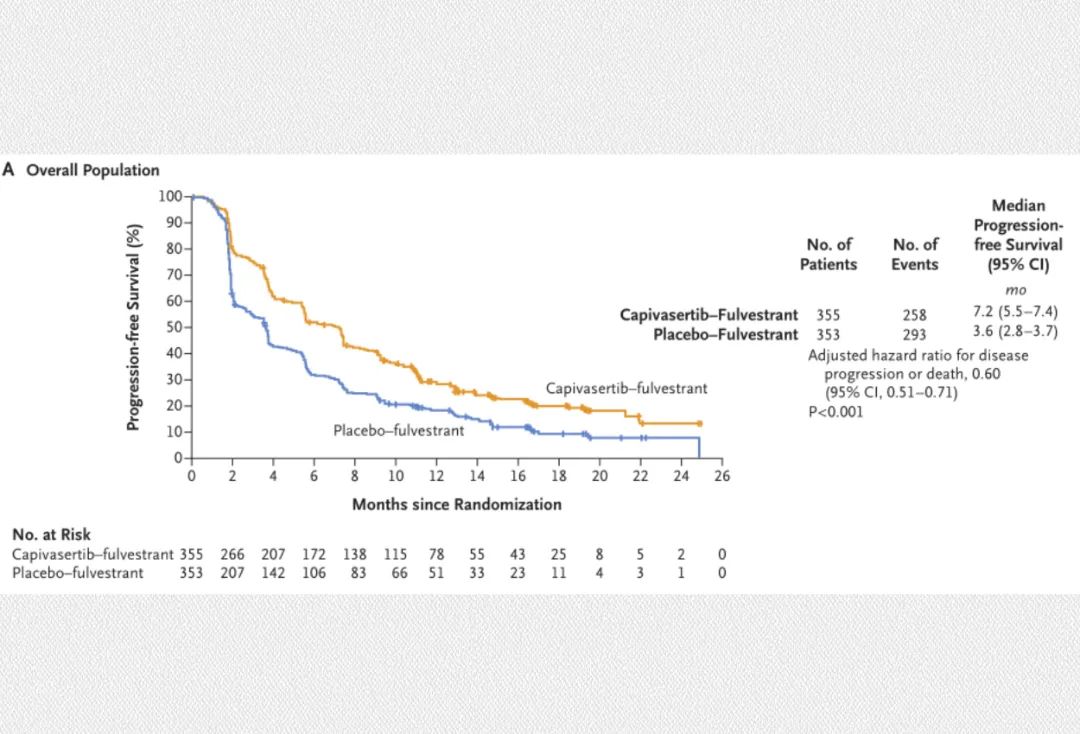

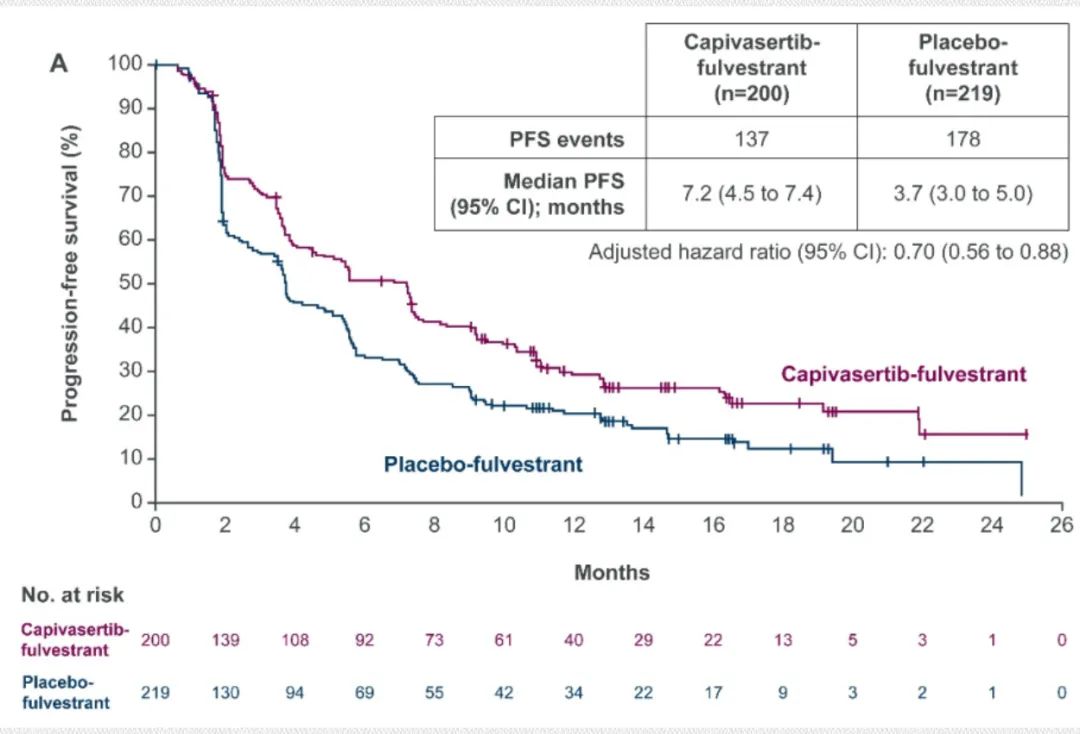
由此可见,患者无论是否接受过CDK4/6抑制剂治疗,Capivasertib+氟维司群组PFS均显著长于单独使用氟维司群治疗;并且无论AKT通路状态如何,患者均与总人群具有一致获益趋势。截至数据截止日期,OS数据尚未成熟,已显示出获益趋势,目前CAPItello-291研究仍在持续随访中。
2023 ASCO:Capivasertib治疗组AE低级别且可控,安全性优势突出
此次ASCO会议披露了CAPItello-291的安全性数据,主要总结了Capivasertib+氟维司群治疗常见AE的发生率、处理方法和发病时间,旨在帮助临床医生详细了解Capivasertib+氟维司群治疗的安全性特征,尽量预防和管理治疗中的毒副作用,为患者提供更安全、有效的乳腺癌治疗方案。
安全性人群包括接受Capivasertib+氟维司群治疗的355名患者和接受安慰剂+氟维司群治疗的350名患者。数据显示,Capivasertib+氟维司群组常见的不良事件是腹泻(72.4% vs. 20.0%)、皮疹(38.0% vs. 7.1%)、恶心(34.6% vs.15.4%)和高血糖(16.3% vs. 3.7%),大多为1~2级AE。约83例患者报告了3级AE,其中皮疹43例(12.1%)、腹泻33例(9.3%)、高血糖症7例(2.0%),整体未发生4级及以上严重AE。在AKT通路改变的人群中,Capivasertib+氟维司群的安全性特征与整体人群相似。

AE导致患者停药的比例率低,分别有28例患者(7.9%)、16例(4.5%)及2例患者(0.6%)因腹泻、皮疹及高血糖症导致两联用药方案剂量减少;35例(9.9%)、42例(11.8%)、9例(2.5%)患者因腹泻、皮疹及高血糖症而中断用药;因严重AE所致的停药率低,因腹泻、皮疹、高血糖停药率分别仅为2.0%、4.5%、0.3%。高血糖患者中约47%(28/60)使用了治疗药物,主要是二甲双胍(n=18)。

经研究者分析,与高血糖症相关的基线风险因素可能包括:Capivasertib+氟维司群组与对照组相比有糖尿病史的患者比例更大(9.6% vs 5.7%) ,以及两组HbA1c基线水平均较高(5.4%[4.0-8.3] vs 5.4% [3.9-7.7])、超重/肥胖患者较多(54.1% vs 53.6%)。另外,CAPItello-291试验采用了间歇性给药方案,这在临床开发早期就被选定,部分原因是为了最大限度地抑制AKT并优化治疗窗口。研究者表示,Capivasertib的毒副作用较低,高血糖发生率较低,也可能与这种间歇性给药方案有关。

总体而言,Capivasertib+氟维司群AE主要发生在治疗早期(1~2周),常见AE腹泻、皮疹、高血糖症的中位发病时间分别为8.0、12.0、15.0天,而且AE通常为低级别且易管理,整体安全性可控,患者耐受性良好。
目前,针对PI3K/AKT/mTOR通路的抑制剂是HR+晚期乳腺癌内分泌治疗及CDK4/6抑制剂耐药后治疗的研究热点,有多项研究正在探索中,mTOR抑制剂、PI3K抑制剂均取得了良好的疗效,为患者带来显著的临床获益10-12,同时常见的不良反应如口腔炎、皮疹、疲劳、腹泻、高血糖等也受到临床关注。Capivasertib治疗后口腔炎(14.6%)和高血糖症(16.3%)的发生率和分级较低,其安全性特征便于临床管理4。在临床实践中,不良反应会在一定程度上影响患者的治疗信心和生活质量,因此,临床医生还应做好不良反应的全程管理,提高对AE的充分认识,改善患者依从性,以达到治疗和获益的持续。
专家点评——张清媛教授:
立鸿鹄之志,后浪新药Capivasertib或将引领First-in-Class AKT抑制剂赛道 1.迄今为止,CAPItello-291研究是全球首个AKT抑制剂用于HR+/HER2-晚期乳腺癌达到双重研究终点的Ⅲ期临床研究,PFS获益结果令人振奋,OS亦有优异获益趋势。而此次公布的安全性分析则显示Capivasertib整体的安全性良好可控,通过对AE的早期识别和干预可以减少3/4级AE发生并提高疗效。目前PI3K/AKT/mTOR通路抑制剂研究已在HR+晚期乳腺癌2线治疗领域取得了较好的结果,为此类患者带来了新的曙光,但安全性管理问题仍需得到重视。Capivasertib≥3级AE发生率较低(皮疹12.1%,腹泻9.3%,高血糖症0.3%),是目前PI3K/AKT/mTOR通路抑制剂中安全性优势更为突出的药物选择。临床医生需要根据不同的AE进行针对性早期预防和管理,以降低严重毒性反应的发生率。总体而言,CAPItello-291研究结果充分显示Capivasertib疗效及安全性俱佳,这无疑给予了临床更多的信心,有望重新定义HR+/HER2-晚期乳腺癌内分泌治疗耐药患者二线治疗新标准。相信在上述突破性成果助力之下,Capivasertib将率先跻身全球First-in-Class(首创)AKT抑制剂赛道,Capivasertib+氟维司群将成为全球首个AKT抑制剂联合方案,为更多内分泌治疗耐药HR+晚期乳腺癌患者带来获益。
2.展骐骥之跃,CAPItello系列研究全面铺陈,有望丰富晚期乳腺癌治疗选择
除CAPItello-291研究外,Capivasertib还开展了CAPItello系列研究,以期进一步探索Capivasertib联合现有治疗方式的疗效和安全性,以及进一步拓宽乳腺癌获益人群。其中CAPItello-292研究13旨在探索Capivasertib+哌柏西利+氟维司群三联方案在HR+/HER2-晚期乳腺癌患者中的疗效和安全性,进一步丰富了HR+/HER2-晚期乳腺癌一线治疗药物选择。其初步结果显示,在HR+/HER2−晚期乳腺癌患者中,Capivasertib+哌柏西利+氟维司群三联方案可耐受,剂量水平之间无明显安全性差异,因此,此三联用药方案将成为目前HR+/HER2-晚期乳腺癌一线治疗新选择的有力竞争者。与此同时,正在进行中的CAPItello-290Ⅲ期研究14旨在评估Capivasertib+紫杉醇对比安慰剂+紫杉醇作为局部晚期或转移性三阴性乳腺癌(TNBC)患者一线治疗的疗效和安全性,以期挖掘Capivasertib在TNBC晚期一线治疗中的价值。期待上述研究探索能够获得更好的试验结果,使得Capivasertib联合治疗方案尽快获得批准并应用于临床,造福更多乳腺癌患者。
3.总结:目前CAPItello-291研究已经证实,无论肿瘤AKT通路是否异常改变,以及患者是否接受过CDK4/6抑制剂治疗,内分泌治疗耐药HR+/HER2-晚期乳腺癌患者均能从Capivasertib+氟维司群治疗中获益,该二联用药方案安全性高、毒副反应可控,将有力保证患者的生活质量,有望重塑HR+/HER2-晚期乳腺癌内分泌耐药治疗新格局。
专家介绍
张清媛 教授
主任医师、二级教授、博士生导师
黑龙江省肿瘤防治研究所所长
哈尔滨医科大学附属肿瘤医院副院长
肿瘤学国家重点专科带头人
国家百千万人才工程入选者
国家突出贡献中青年专家
中国抗癌协会乳腺癌专业委员会副主任委员
中国临床肿瘤学会乳腺癌专家委员会副主任委员
中国抗癌协会淋巴瘤专业委员会主任委员
中国抗癌协会化疗专业委员会副主任委员
黑龙江省抗癌协会乳腺癌专业委员会主任委员
参考文献:
-
生物医药领域要点速览

生物医药领域要点速览
-
Cell Res:把肝癌变成“慢病”!厦门大学林圣彩等团队发现“辟谷精”为肝癌治

Cell Res:把肝癌变成“慢病”!厦门大学林圣彩等团队发现“辟谷精”为肝癌治
-
Nature全新子刊—Nature Hearth,上线首篇论文!

Nature全新子刊—Nature Hearth,上线首篇论文!
-
《科学》:癌细胞喜欢“酸”的原因找到了!这种环境让肿瘤生长更猛烈!

《科学》:癌细胞喜欢“酸”的原因找到了!这种环境让肿瘤生长更猛烈!
-
CRM:这思路,绝了!中国医大/浙大/复旦团队,将中性粒细胞变成“顺风车”,搭载

CRM:这思路,绝了!中国医大/浙大/复旦团队,将中性粒细胞变成“顺风车”,搭载