小鼠乳腺癌细胞66c14荧光素酶标记肿瘤模型
模型制作方法:
1、表达载体构建:构建chicken β-actin-luc-NEO载体CAG启动子由巨细胞病毒(the cytomegalovirus,CMV)早期增强子(early enhancer element)和鸡β-肌动蛋白(chicken beta-actin )启动子组成,用于驱动基因在哺乳动物载体的高水平表达。
2、66c14-Luc荧光细胞系的获得:采用脂质体2000转染小鼠乳腺癌细胞66c14细胞,转染后24 h,用含有G418的培养液筛选细胞三周,获得稳定表达luciferase的细胞株,选择其中高表达的克隆株扩大培养。
3、肿瘤细胞的植入及活体荧光成像:收集处于生长对数期的转染细胞,稀释至5×106/mL。取0.1 mL细胞悬液接种于BALB/c小鼠(5周龄,体重15-18 g)右侧第二对乳腺脂肪垫内。1×106个细胞/只,接种后每隔一周,采用活体荧光影像系统摄像动态观察肿瘤的生长和转移情况。观察前每只小鼠腹腔注射荧光素底物(1.5 mg/10 g),饱和三溴乙醇(0.18 mL/10 g)麻醉后放人活体荧光影像系统摄像,Slide Book 4.0软件进行分析。
模型表型数据:
本模型将luc基因转染到小鼠乳腺癌细胞66c14中得到了高表达luciferase细胞株。经过多次传代表达水平稳定,标记细胞的形态、生长方式、生长速度及致瘤能力等与未转染细胞无明显差异,可以反映小鼠乳腺癌细胞66c14肿瘤细胞生物学行为的标记细胞。
将Luc标记的小鼠乳腺癌细胞66c14细胞经皮下接种至BALB/C小鼠,用活体荧光成像系统连续观察,发现14d能够成瘤,28d肿瘤面积显著增大,48d后原位肿瘤面积变小,但能够观察到明显的肺转移及其它脏器的转移(图1),建立了一种新的能够用于活体内连续监测肿瘤生长的动物模型。
此模型与常规模型相比具有以下优点:
1)无创伤性;
2)可多次重复在不同时间点检测;
3)快速扫描成像(时间少于5 min);
4)可以使实验动物整体成像;
5)同一实验动物体内获得全部时间点的整体数据。
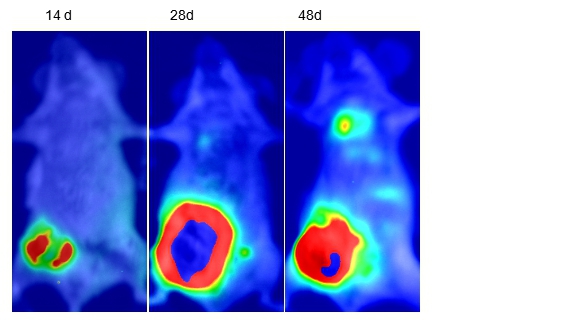
图1 小鼠乳腺癌66C14小鼠乳腺原位接种
66c14与4T1和4T07细胞模型比较。将Luc标记的4T1、66c14、4T07细胞对BALB/c小鼠乳腺原位接种4T1细胞乳腺原位移植瘤最大,66c14细胞瘤体次之,4T07细胞瘤体最小;接种后35 d,三株细胞乳腺原位移植瘤大小较一致。4T1和66c14原位移植瘤均可发生转移,其中4T1细胞较66c14细胞转移最为严重,而4T07细胞未见转移。
乳腺癌原位自发转移模型较尾静脉转移模型更真实反应了肿瘤细胞在体的转移特性,且能完整地呈现肿瘤转移的全过程,可作为研究肿瘤转移的最理想模型。
-
江西中医药大学/深圳市人民医院等联合发表14.6分Top期刊,揭示迷迭香酸通过调

江西中医药大学/深圳市人民医院等联合发表14.6分Top期刊,揭示迷迭香酸通过调
-
超详细教程:论文图片要求有哪些,图片配色怎么调

超详细教程:论文图片要求有哪些,图片配色怎么调
-
SCI投稿:全流程详细指南

SCI投稿:全流程详细指南
-
一年中SCI黄金投稿期,终于被我拿捏了!

一年中SCI黄金投稿期,终于被我拿捏了!
-
干货 || 活细胞表面抗原的荧光染色(间接免疫荧光)

干货 || 活细胞表面抗原的荧光染色(间接免疫荧光)